E honlap szerkesztője szeretett volna egy összefoglaló tanulmányt keresni az interneten a HPV (Human Papilloma Vírus) védőoltással kapcsolatos kérdéskörről. Azonban olyan tömegű információ jött velünk szembe, hogy szinte lehetetlen egy tanulmányban átfogó helyzetjelentést adni.
Így most azt célozzuk meg, hogy önkényesen kiválasztunk egy tanulmányt, amelyről úgy gondoljuk, hogy jól összefoglalja a helyzetet, egy későbbi bejegyzésben pedig további, az interneten elérhető információkra utalunk rövid formában.
Mindenekelőtt fontoljuk meg a következőket:
Az oltóanyagipart nem az emberek egészségének megőrzése, hanem a profit maximalizálása vezérli. Nem a koviddal kezdődött, de a kovid-jelenség világosan megmutatta, hogy a cél érdekében a gépezet képes volt adatok hamisítására, az engedélyező hatóságok korrumpálására, és képes volt holttesteken is átgázolni. Megtapasztaltuk továbbá, a kovidjelenséget sok év alatt mindenre kiterjedő figyelemmel és aprólékos munkával készítették elő, a hibavétés lehetőségét gyakorlatilag teljesen kizárva. Ugyancsak szembe kell vele néznünk, elképzelhető, hogy a profitmaximalizálás ugyan fontos célja volt az akciónak, de lehet, hogy voltak más szempontok is, úgy mint a gazdaság tönkretétele, államadósságok növelése, a társadalmak egészségi állapotának gyengítése a teljes ellenőrzés bevezetése, és nem utolsósorban eugenikai szempontok is játszhattak szerepet, értsd, a háttérhatalom a kívánatos népességcsökkentés eszközeként vetette be a kovidoltás fegyverét.
Nos, ha ez így van a kovidnál, akkor kényszerítő, hogy ezek az attribútumok már a kovid előtt, tehát például a HPV-vakcinánál is megvoltak.
Ezeket előrebocsátva adjuk közre Norma Erickson und Peter H. Duesberg, PhD cikkét:
Mi van, ha a HPV nem okoz méhnyakrákot?
A cikk az oltások mellékhatásairól tájékoztató https://sanevax.org/ honlapon jelent meg 2015-ben.
Egy, a McCormack és munkatársai által a Molecular Cytogenetics-ben 2013-ban megjelent tanulmány címe mindent elmond: „Egyéni kariotípusok a méhnyak karcinómák képződményeinél„. Ha a tanulmány megállapításai igazak, akkor rendkívül valószínűtlen, hogy a humán papillomavírus (HPV) elleni vakcina védelmet nyújt a méhnyakrák ellen.
A tanulmány szerint sem a genetikai hajlam, sem a HPV-fertőzés nem szükséges a méhnyakrák kialakulásához. A vizsgálat során vizsgált összes méhnyakrákos sejt új abnormális kariotípusokat tartalmazott. Ezeknek az új abnormális kariotípusoknak a klonálitása (genetikai felépítése) azt jelzi, hogy a méhnyakrák ezekből a kariotípusokból származik – NEM vírusból.
Annak érdekében, hogy megértsük ezeknek az állításoknak a potenciális jelentőségét, alapvető ismeretekkel kell rendelkeznünk a kariotípusokról. A legtöbb élőlény sejtjeiben kromoszómák vagy genetikai információs egységek vannak. A kromoszómák száma és megjelenése fajonként változik. A kariotípus a kromoszómák száma, mérete és alakja bármely adott szervezetben.
Lásd az emberi kariotípus grafikus ábrázolását jobbra. Minden embernek 23 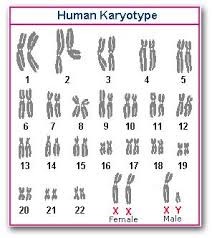 pár kromoszómája van (összesen 46), amint azt az ábra mutatja, a jobb alsó sarokban látható utolsó pár határozza meg az adott ember nemét. Bármely más szám más fajt jelezne. Például a majmoknak 48 kromoszómájuk van, a kenguruknak pedig 20. Bármely adott sejtben lévő kromoszómák száma, mérete és alakja felfedi az adott sejt származási faját.
pár kromoszómája van (összesen 46), amint azt az ábra mutatja, a jobb alsó sarokban látható utolsó pár határozza meg az adott ember nemét. Bármely más szám más fajt jelezne. Például a majmoknak 48 kromoszómájuk van, a kenguruknak pedig 20. Bármely adott sejtben lévő kromoszómák száma, mérete és alakja felfedi az adott sejt származási faját.
A rákspecifikus kariotípusok magyarázata
Minden ráknak egyedi klonális (az anyasejtből származó és genetikailag azonos sejtek) kariotípusai (a kromoszómák száma, mérete és alakja), és így fenotípusai (kifejezett fizikai tulajdonságok) vannak. Nincs két egyforma rák. Lásd a kariotípus mezőket (array) a fent említett és a cikk végén hivatkozott tanulmányban.
A kariotípus több ezer (kromoszómánként körülbelül ezer) hírvivő RNS segítségével határozza meg a fenotípust, amelyek viszont több ezer fehérjét termelnek – rákos kariotípus-specifikus koncentrációkban (kópiaszámokban). Minden rákos sejt nagyon különbözik egyénileg a normál sejtektől. Ebben a tekintetben a rákos sejtek hasonlítanak az emberi testben létező új sejttípusokra, hasonlóan egy parazitához.
A rákos sejtekben lévő gének és fehérjék nagyon abnormális koncentrációban exprimálódnak az őket körülvevő normál sejtekhez képest. Mivel azonban a rákos sejtekben exprimálódó összes gén és fehérje emberi sejtekből származik, a rákok nem immunogének (nem képesek immunválaszt kiváltani) – annak ellenére, hogy hatalmas biológiai különbségek vannak a környező normál sejtektől. Ez az oka annak, hogy az immunrendszer nem „látja” a rákot.
Mivel az új karcinóma kariotípusok több ezer normális gént hoznak létre rendellenesen, számos új rákspecifikus fenotípust generálnak, amelyek egy-egy az egyben korrelálnak a rákos sejtek új kariotípusaival. A méhnyakrákos sejtek egy példa.
Gondoljunk a Down-szindrómára, mint modellre; Egy extrém kicsi 21-es kromoszóma sokmindent meghatároz. (A Down-szindróma azt jelenti, hogy a 21. sz. kromoszómából 2 helyett 3, tehát eggyel több van.) A rákok jellemzően 60-70 kromoszómavariációval rendelkeznek, szemben a Down-szindróma 46 + 1 kombinációjával.
Hipotézis: A humán papillomavírus (HPV) méhnyakrák okoz
Ez a hipotézis azt állítja, hogy a HPV olyan fehérjéket kódol, amelyek rákot okoznak, amikor a vírus replikálódik. A közös transzformációs fehérjékkel az összes méhnyakkarcinóma többé-kevésbé azonos lenne, ha ez pontos lenne. Mivel a vírusfehérjék idegenek az embertől, a vírusok, a vírussal fertőzött sejtek és esetleg a vírus-transzformált tumorsejtek elkerülhetetlenül immunogének lennének, és mint ilyenek, a gazdaszervezet immunrendszere a fertőzést követő heteken vagy hónapokon belül kiürülne.
Ez az oka annak, hogy a HPV által kiváltott szemölcsöket az immunrendszer a fertőzés után heteken vagy hónapokon belül megszünteti.
Ez a hipotézis négy kérdést vet fel:
- Miért csak 10 000 HPV-fertőzött nőből 1-nél alakul ki méhnyakrák?
- Miért csak 20-50 évvel a fertőzés után alakul ki méhnyakrák? Más szóval, miért nem akkor okoz a vírus rákot, amikor biokémiailag aktív és szemölcsöket okoz, mielőtt a természetes vírusellenes immunitás semlegesítené?
- Miért különböznek egymástól a méhnyaki karcinómák a malignitás, a gyógyszerrezisztencia és a sejtszövettan (hisztológia) szempontjából, amint azt eredetileg Papanicolaou és munkatársai 1952-ben leírták a Science-ben, ha ugyanazok a vírusfehérjék okozzák őket?
- Miért nem immunogének azok a méhnyakkarcinómák, amelyeket feltehetően a humán papillomavírus fehérjék generálnak, és így nem ürülnek ki természetes antitestekkel?
Annak ellenére, hogy több mint 25 éve kutatják a HPV – rák összefüggést, nincs közvetlen válasz ezekre a kérdésekre.
Ehelyett a rosszul definiált „kofaktorokat” neveznek ki a HPV „együttműködőiként” a karcinómák okaiként. A HPV-negatív nők méhnyakkarcinómáinak okaként rosszul definiált sejtmutációkat emlegetnek.
Ráadásul a méhnyakrák mintegy 30% -ban vírusmentes. Ezekben az esetekben a vírus még elméletileg sem lehet felelős a rákért.
A méhnyakrák kialakulásának kariotípusos ráksejttípus-képződést feltételező elmélete
A McCormack et al. tanulmánya, „Individual kariotypes at the origins of cervicalis carcinomas” (Egyéni kariotípusok a méhnyakkarcinómák eredeténél) továbbfejleszti azt az elméletet, hogy a karcinogenezis a ráksejttípus (faj) képződés egyik formája (Lásd Duesberg et al., „Is carcinogenesis a form of speciation? = A karcinogenezis a ráksejttípus (faj) képződésnek egy formája?” Cell Cycle 2011).
Ezen elmélet szerint a kariotípusos evolúció új ráktípusokat (fajokat) hoz létre a normál sejtekből rákkeltő anyagoknak (pl. cigarettafüst vagy röntgensugárzás) való kitettség vagy spontán mitotikus balesetek után. A rákkeltő anyagok közös jellemzője az aneuploidia (kromoszóma-zavar, nyereség vagy veszteség) indukálása. Több ezer gén kiegyensúlyozatlanságával az aneuploidia automatikusan destabilizálja a normál emberi sejt kariotípust, és így katalizálja a véletlenszerű kariotípusos variációkat. A proliferatív fenotípusú variánsok szelekciója nem-klonális pre-neoplasztikus hiperpláziákat (nem neoplasztikus sejtek fokozott növekedése egy szövetben vagy szervben) képez, tartósan változó kariotípusokkal. Nagyon ritka kariotípusos variációk autonóm (a környező gazdasejtek befolyása nélkül képesek replikálódni) új ráktípusokat alkotnak egyedi klonális kariotípusokkal. A rák kariotípusait szűk variációs határokon belül stabilizálódnak klonális szelekcióval a rákspecifikus autonómia érdekében. Mivel ez a mechanizmus nagyon kevéssé hatékony, a rákkeltő expozíciótól számítva hosszú látens időszakokat jelez előre az egyes klonális kariotípusos rákos megbetegedésekre.
Ezzel az elmélettel összhangban a szerzők új, rákspecifikus kariotípusokat és fenotípusokat fedeztek fel az összes eddig vizsgált méhnyakkarcinómában – mind HPV-DNS-pozitív, mind negatív karcinómákban.
Továbbá felfedezték, hogy az egyes karcinómák egyedi kariotípusai 1:1-ben megfelelnek az egyéni fenotípusaiknak (pl. invazivitás és kemoterápiás gyógyszerekkel szembeni rezisztencia). Ez elvi bizonyíték arra, hogy ezek a kariotípusok határozzák meg a rák fenotípusait – nem pedig a hibás és látens papilloma-vírus DNS-ek.
A kariotípusos ráksejttípus-keletkezés elmélet szerint a „HPV DNS-pozitív” karcinómák hibás vírus DNS-ei funkcionálisan irrelevánsak, mivel nem exprimálnak vírusfehérjéket. Ehelyett nem immunogén fosszíliák, amelyek régmúlt papilloma-vírus fertőzésekből származnak. Mint ilyenek, nem felelnek meg annak a több ezer sejtgénnek, amelyek rendellenesen exprimálódnak a méhnyakkarcinómákban.
A kariotípusos sejttípus elmélet megmagyarázza a HPV – rák hipotézis paradoxonjait
Miért csak 1 nőnél alakul ki méhnyakrák 10 000 HPV-fertőzés esetében?
A kariotípusos karcinóma elmélet szerint ez az eltérés annak a ténynek az eredménye, hogy a HPV-fertőzés és a karcinogenezis két teljesen független esemény:
- Nincs specifikus összefüggés a HPV és a méhnyak karcinóma között. A HPV nagyon gyakori, körülbelül 70-80% endémiás az amerikai népességben. A lakosság többi része HPV-mentes. A vírus jellemzően fiatal korban szexuális úton terjed. Mivel a méhnyakkarcinómák mind HPV-pozitív, mind HPV-negatív nőknél előfordulnak, nincs specifikus korrelatív bizonyíték arra, hogy a HPV bármilyen szerepet játszik a méhnyakrák kialakulásában.
- Nincs specifikus funkcionális összefüggés a HPV-fertőzés és a karcinogenezis között sem. Amint azt a méhnyakrák klonális kariotípusai mutatják, a rákok a normál sejtek kariotípusainak jelentős átrendeződéséből származnak. Mivel ez igaz a HPV-pozitív és HPV-negatív nők méhnyakkarcinómáira – és valóban igaz minden rákra -, nincs funkcionális bizonyíték arra, hogy a HPV szerepet játszik a karcinómák kialakulásában. Ez a következtetés összhangban van azzal a ténnyel, hogy az új klonális kariotípusokkal rendelkező karcinómák csak 20-50 évvel (!) a HPV-fertőzés után jelentkeznek, amelyet a következőkben tárgyalunk.
Így nincs specifikus összefüggés a jelenlét és/vagy a funkciók között; vagy a HPV és a karcinogenezis funkcióinak hiánya.
Miért csak 20-50 évvel a HPV-fertőzés után alakul ki méhnyakrák?
A kariotípusos rák elmélet megmagyarázza a HPV-fertőzéstől a rákig terjedő feltételezett hosszú lappangó időszakot. Ez a hatalmas lappangó időszak két, egymástól teljesen független esemény bizonyítékát sugallja:
- Szexuális úton terjedő, jóindulatú humán papillomavírussal való fertőzés fiatal korban, és
- Méhnyakrák diagnózis – amelynek 90% -a 50 éves kor felett fordul elő.
A feltételezett hosszú látens időszak annak az alacsony valószínűségének az eredménye lehet, hogy egy normál szomatikus sejtből véletlenszerű kariotípusos átrendeződésekkel új autonóm ráktípus jön létre. Egy új, egyedi sejttípus (méhnyakrákos sejtek) evolúciója, amely képes a környező emberi sejtek befolyásától függetlenül szaporodni a prekurzor sejtek véletlenszerű kariotípusos variációival, időbe telik.
Egy új, autonóm ráksejttípus véletlenszerű kariotípusos evolúcióval történő kifejlődésének nagyon alacsony valószínűsége nemcsak a HPV-fertőzés (ha előfordul) és a méhnyakkarcinóma közötti hosszú és kiszámíthatatlan időintervallumokat magyarázza, hanem az összes rák klasszikus életkori torzítását is. A rák életkori torzítása azt mondja, hogy az összes rák több mint 90% -a csak 50 év feletti korban fordul elő.
A szerzők arra a következtetésre jutottak, hogy a HPV-fertőzés és a karcinogenezis közötti kronológiai eltérések kizárják a vírusfertőzés és a rák kialakulása közötti közvetlen hatásmechanizmust. Ehelyett egy új rákspecifikus kariotípus időfüggő evolúciója támogatja a méhnyakkarcinómák eredetének kariotípusos elméletét.
Miért vannak a méhnyakkarcinómáknak egyedi kariotípusai és fenotípusai – a vírus hipotézise által előre jelzett közös fenotípusok helyett?
Annak a valószínűsége, hogy egy új autonóm ráksejttípus kariotípusát véletlenszerű kariotípus-variációkkal alakítsuk ki, nagyon alacsony, és így valószínűtlen, hogy ugyanazt az új sejttípust kétszer hozza létre – ugyanúgy, mint a hagyományos fajoknál. Így a kariotípusos species által okozott összes ráknak egyedi, még ha néha hasonló fenotípusai is lesznek.
Miért nem immunogének az állítólagos vírusos méhnyakkarcinómák, és így nem eliminálódnak természetes antitestekkel?
A kariotípusos speciációs elmélet megmagyarázza, hogy a feltehetően vírusos méhnyakkarcinómák miért nem immunogének, és így képesek növekedni HPV-DNS-pozitív emberekben, amelyek HPV-ellenes antitesteket tartalmaznak, amelyek a vírus korábbi fertőzésének (fertőzéseinek) eredményeként termelődnek.
A kariotípusos rákelmélet szerint a karcinómákat de novo generálják celluláris kromoszómákból, génekből és fehérjékből, amelyek nem immunogének a származási gazdában (csakúgy, mint minden más rák). Ezzel szemben a vírusfehérjék által generált hipotetikus rákos sejteket az antivirális immunitás azonnal fölszámolná.
Mivel a méhnyakkarcinómák klonális karcinóma-specifikus kariotípusokkal rendelkeznek, tudjuk, hogy több ezer normál sejtgén kromoszóma-átrendeződésével jöttek létre, amelyek nem immunogének.
A szerzők szerint az inert HPV DNS töredékei, amelyek a méhnyakrák 70-80% -ában találhatók (és az Egyesült Államokban az összes nő 70-80% -ában!) a karcinogenezis előtt 20-50 évvel bekövetkezett múltbeli fertőzések vagy szemölcsök maradványai. A fertőzéseket és az ebből eredő tüneteket természetes HPV-ellenes antitestekkel szüntették meg.
Ha a kariotípusos ráksejttípus kialakulás elmélet helyesnek bizonyul, a HPV vakcinák valószínűleg nem csökkenthetik a méhnyakrák – vagy bármely más típusú rák – előfordulását.
Mit tegyünk most?
Amíg a tudósok nem tudják igazolni vagy megcáfolni a méhnyakrák kialakulásának kariotípusos fajkialakulás elméletét, az orvosoknak és pácienseknek óvatosan kell eljárniuk.
Ez egy tudományos vita, amelyet nem lehet figyelmen kívül hagyni. A közegészségügyi hatóságoknak és az egészségügyi szakembereknek az elővigyázatosság elvét kell alkalmazniuk a HPV vakcinák használatának felfüggesztésével és a méhnyakrák elleni védekezés már bizonyított, biztonságos és hatékony módszerének, a Pap-szűrésnek a támogatásával.
Ez az a módszer, amely George Papanicolaou et al. 1952-ben a Science-ben történő publikálása majd bevezetése után csökkentette a méhnyakrák előfordulását az Egyesült Államokban a nők 10 leggyakoribb ráktípusainak listájából arra a helyre, amely már nincs a listában.
Ráadásul ez a méhnyakkarcinómák bizonyított tesztje, amelyet Papanicolaou után Pap-szűrésnek neveznek, csak egy kis töredékébe kerül a Gardasil és a Cervarix vakcinák 300-500 dollárjának, és NINCS komoly káros hatása.
Azonnali független tanulmányokat kell végezni annak felfedezésére, hogy a fent tárgyalt elméletek közül melyik helyes. Ha a HPV nem okoz rákot – a HPV vakcinák haszontalanok.
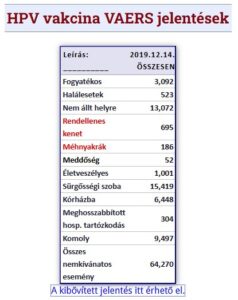
Kép forrása: https://sanevax.org/hpv-not-cause-cervical-cancer/
Ha a HPV vakcinák haszontalanok, akkor biztosan nem érdemes alávetni magunkat (vagy szeretteinket) a súlyos mellékhatások 2,3-2,5% -os kockázatának ÉS egy új betegség kialakulása 2,4-3,3% -os kockázatának sem, amely potenciálisan a Merck Gardasil 9 klinikai vizsgálatának résztvevői által tapasztalt autoimmun rendellenességekre utal.
MAXIMÁLIS KOCKÁZAT, MINIMÁLIS HASZON – SEMMILYEN KÖRÜLMÉNYEK KÖZÖTT NEM BÖLCS ORVOSI VÁLASZTÁS.
Hivatkozások:
Egyéni kariotípusok a méhnyakrákok kialakulásakor (McCormack és mtsi.; Molecular Cytogenetics, 2013)
A klonalitás értékelése humán tumorokban: Áttekintés (CANCER RESEARCH 50, 135-1360, 1990. március)
A rákok újonnan kifejlődött fajok? (Robert Sanders, UC Berkeley, 2011)
Vírusok: Struktúrák, funkciók és alkalmazások (Molekuláris sejtbiológia, 4. kiadás)
A karcinogenezis a fajképződés egy formája (Duesberg et al., Cell Cycle 2011)
Az FDA által jóváhagyott Gardasil 9: Hűtlen kezelés vagy ostobaság? (Erickson, 2014)
A Gardasil 9 betegtájékoztatója.
Közzétevőnek van némi problémája avval a felfogással, hogy a rákos sejteket önálló, új fajnak tekintik. De közzétevő nem biológus, és ha a biológus társadalom ezt elfogadja, akkor tudomásul veszi.
2024. január
Fordította:
Király József

Kétezer körül a Fidesz kormány ingyen biztosította a fiatal lányoknak a HPV elleni oltást. akkoriban nagyon akartam a lányomnak, de valamiért lemaradtunk az ingyenes adagról. SZERENCSÉRE, mondom most már.
Meg 2000 után is. A kisebbik lányom a hetedik osztályban volt várományosa ennek az oltásnak. A több évfolyamból mindössze ketten voltunk szülőpárok, akik utánanéztünk ennek az oltásnak, és köszöntük nem kértük. Látni kellett volna a többi szülőt, milyen fejet vágtak erre…mindezt úgy, hogy fogalmuk sem volt arról, hogy az állítólagosan rákot okozó vírustörzsek közül (amiből vagy 10-16 féle volt állítólag) mindössze négy ellen nyújtott állítólagos védelmet a vakcina, azt is csak öt évig, azaz ötévente újra kellett volna oltani a teljes társaságot, az állítólagos védelem fenntartására. És akkor még nem beszéltünk arról, hogy vajon hány hpv-oltott gondolja azt, hogy ő aztán most egész életében védett a vírus és ezáltal a méhnyakrák ellen és aztán emiatt el se megy mondjuk rákszűrésre, mert minek az…